发布时间:2026-03-18 10:43:06 来源: 浏览次数:170
《儿科药学杂志》 2026 年第 32 卷第 3 期
β 受体阻滞剂联合聚桂醇治疗婴幼儿血管瘤的临床研究
漆召阳,王鑫,赵艺 (自贡市第一人民医院,四川自贡 643000)
摘要:目的:探讨 β 受体阻滞剂联合聚桂醇治疗婴幼儿血管瘤(IH)的疗效及其对血清色素上皮衍生因子(PEDF)、基质金属蛋白酶-9(MMP-9)水平的影响。
方法:选取我院 2022 年 10 月至 2024 年 5 月收治的 90 例 IH 患儿,按随机数表法分为常规组(单用 β 受体阻滞剂阿替洛尔)和联合组(阿替洛尔联用聚桂醇)各 45 例。 比较两组患儿的疗效、安全性、瘤体面积和厚度变化及血清血管内皮生长因子(VEGF)、碱性成纤维细胞生长因子(bFGF)、转化生长因子-β1(TGF-β1)、PEDF、MMP-9 水平。
结果:联合组总有效率为 95. 56%,高于常规组的 77. 78%(P<0. 05)。 治疗后,两组患儿血管瘤面积、厚度均减小,血清 TGF-β1、bFGF、VEGF、MMP-9 水平降低,而 PEDF 水平升高(P<0. 05),联合组上述指标的变化幅度均大于常规组(P<0. 05)。 联合组与常规组不良反应发生率比较差异无统计学意义(P>0. 05)。
结论:阿替洛尔与聚桂醇联合治疗 IH,可显著提升疗效,并有效调节患儿血清中 PEDF 水平及降低 MMP-9 水平。
关键词:β 受体阻滞剂;聚桂醇;婴幼儿血管瘤;色素上皮衍生因子;基质金属蛋白酶-9
doi:10. 13407 / j. cnki. jpp. 1672-108X. 2026. 03. 004
婴幼儿血管瘤( infantile hemangioma,IH) 是儿科领域常见肿瘤,影响约 5%新生儿,发病率为 2% ~ 10%[1]。虽为良性,但 10% ~ 15%可能引发皮肤扩张、溃疡、坏死(面部病变尤甚)[2]。 既往治疗手段有限且效果不均,手术对婴幼儿风险较大及恢复问题较多;随着研究深入,药物治疗成为主流,β 受体阻滞剂作为一线药物,通过阻断 β 受体调节血管舒缩、抑制内皮细胞增殖以控制瘤体,临床效果显著[3]。 但鉴于患儿对药物反应存在个体差异,部分患儿的治疗效果往往难以达到理想状态[4]。聚桂醇作为新型硬化剂,可使血管内皮细胞变性坏死、血管闭塞,导致瘤体纤维化萎缩,但单独用于较大或深部血管瘤治疗时,可能有局部组织损伤、感染等风险[5]。聚桂醇与 β 受体阻滞剂协同,可降低前者系统性不良反应及后者局部损伤风险,尤其对特殊部位或较大深部IH,能增强瘤体控制效果,为解决单一疗法的局限及为高风险难题的解决提供了新路径。 色素上皮衍生因子(pigment epithelium derived factor,PEDF) 是有效血管形成抑制因子,兼具抑制新生血管、抗肿瘤、神经保护等功能[6]。基质金属蛋白酶-9 ( matrix metalloproteinase-9,MMP-9)通过降解细胞外基质促进血管生成和肿瘤侵袭,与血管瘤增殖密切相关[7],二者均在血管瘤发生、发展中发挥着重要作用。 因此,本研究通过探讨 β 受体阻滞剂联合聚桂醇治疗 IH 的疗效及其对 PEDF、MMP-9 水平的影响。
一、资料与方法
1.1 一般资料
样本量计算见公式(1)。 式中,n 为每组所需样本量,π1 为常规组预期有效率( 65. 00%,基于前期预实验),π2 为联合组预期有效率( 90. 00%,基于前期预实验),Ⅰ类错误( α) = 0. 05,Ⅱ 类错误 ( β) = 0. 2,查得f(0. 05,0. 2)= 7. 9。 代入计算得 n = 40,考虑 10%脱落率后每组至少需纳入 44 例。
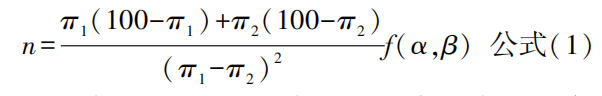
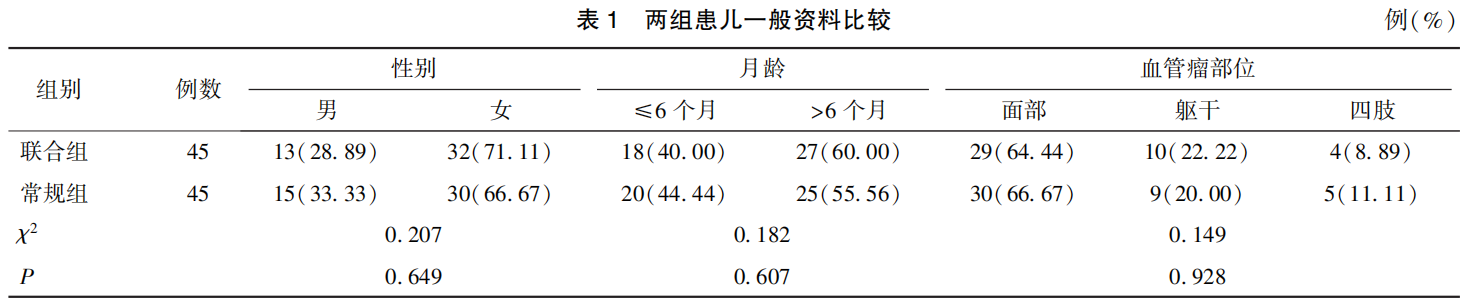
选取 2022 年 10 月至 2024 年 5 月我院收治的 90 例IH 患儿,按随机数表法分为常规组和联合组各 45 例。两组患儿性别、月龄、血管瘤部位比较差异无统计学意义(P>0. 05),见表 1。 本研究通过我院医学伦理委员会审查[伦理(M)2022-029],患儿监护人已签署知情同意书。 纳入标准:(1)符合《血管瘤和脉管畸形的诊断及治疗指南(2019 版)》[8]中 IH 诊断标准,依据病史、临床和影像学确诊;(2)年龄 2~ 12 个月;(3)血常规、凝血功能基本正常。 排除标准:(1)合并心、肝、肾等重要脏器功能障碍;(2)存在先天性甲状腺功能减退症;(3)严重先天性心脏病;(4)对 β 受体阻滞剂或聚桂醇过敏或存在禁忌证;(5)近 1 个月内接受过其他血管瘤治疗;(6)合并血液系统疾病、自身免疫性疾病或恶性肿瘤。
1.2 治疗方法
常规组采用 β 受体阻滞剂治疗,口服阿替洛尔(国药准字 H12020259,天津市中央药业有限公司,规格:12. 5 mg),初始剂量 0. 5 mg / ( kg·d),根据患儿耐受情况逐渐增加剂量至 1 ~ 2 mg / ( kg·d),平均使用剂量约1. 42 mg / (kg·d),持续用药 6 个月。 停药指征为完成6 个月治疗且血管瘤瘤体缩小≥51%、出现严重不良反应或瘤体提前缩小≥76%。
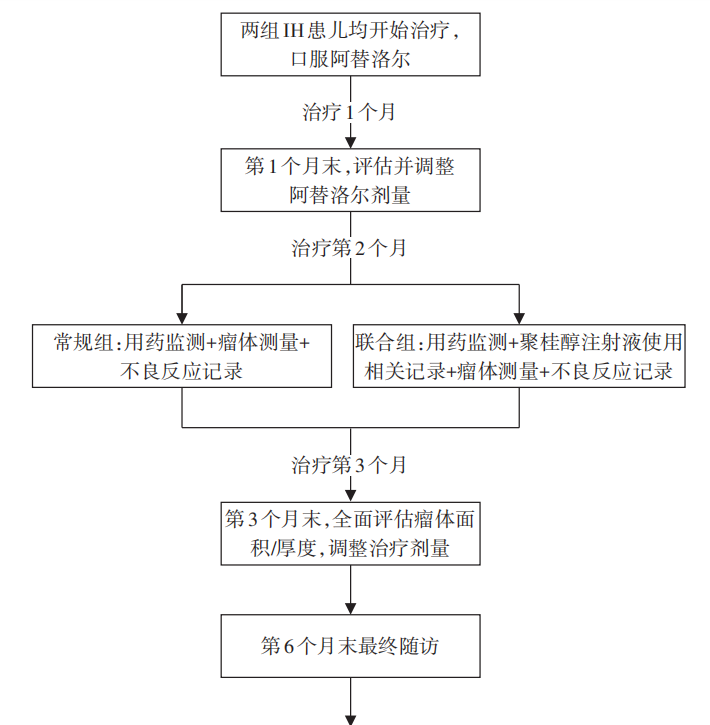
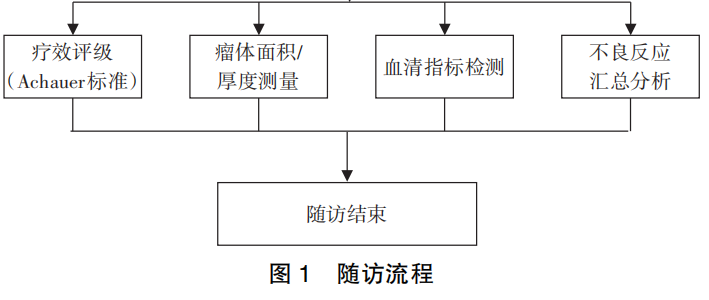
联合组采用 β 受体阻滞剂联合聚桂醇治疗,阿替洛尔用法同常规组。 在阿替洛尔治疗 1 个月后,采用聚桂醇注射治疗(国药准字 H20080445;陕西天宇制药有限公司;10 mL ∶ 100 mg),根据血管瘤瘤体大小及部位,在超声引导下将适量聚桂醇注射液缓慢注入瘤体内,在多个位点进行浸润注射,直至瘤体组织颜色变得苍白,最大剂量每次<6 mL,1 次治疗未消除者,于 2 周后再次注射,总注射次数不超过 2 次。 停药指征为瘤体缩小≥76%或缩小 51% ~ 75%且 2 周无进展,出现不可耐受不良反应,或患儿监护人主动要求停药。 两组患儿均随访 6 个月(图 1),治疗期间按注射周期及用药要求定期随访监测,治疗结束后进行疗效与安全性评估,患儿均完成随访无失访。
1.3 观察指标
1. 3. 1 疗效评价 参考Achauer标准对治疗效果进行评价[9],见表 2。

1. 3. 2 血管瘤状态 治疗过程中嘱患儿来院复诊,在标准光照条件下,使用同一高精度数显卡尺进行测量。测量血管瘤面积时,分别测量瘤体的最长径( a)和与之垂直的最宽径(b),按照公式 S =πΧ(a / 2) Χ(b / 2)计算近似椭圆面积。 测量血管瘤厚度时,选取瘤体最突出处进行。 所有测量均进行 3 次,取平均值记录。
1. 3. 3 血清指标 分别于治疗前及治疗 6 个月后,晨起采集患儿空腹静脉血 3 mL,离心分离血清,严格按照武汉伊莱瑞特生物科技股份有限公司提供的酶联免疫吸附试剂盒说明书操作,测定血清转化生长因子-β1( transforming growth factor-β1,TGF-β1)、碱性成纤维细胞生长因子(basic fibroblast growth factor,bFGF)、血管内皮生长因子( vascular endothelial growth factor,VEGF)、PEDF、MMP-9 水平。
1. 3. 4 不良反应 观察并记录两组患儿治疗期间出现的不良反应,如血压异常、心率减慢、色素沉着、注射部位不适(疼痛、红肿)、浅表性瘢痕等。
1.4 统计学方法
应用 SPSS 21. 0 统计学软件,计量资料以 -x±s 表示,同组治疗前后组内比较采用配对 t 检验,两组组间比较采用独立 t 检验;计数资料以百分率表述,行 χ2 检验,P<0. 05 为差异有统计学意义。
二、 结果
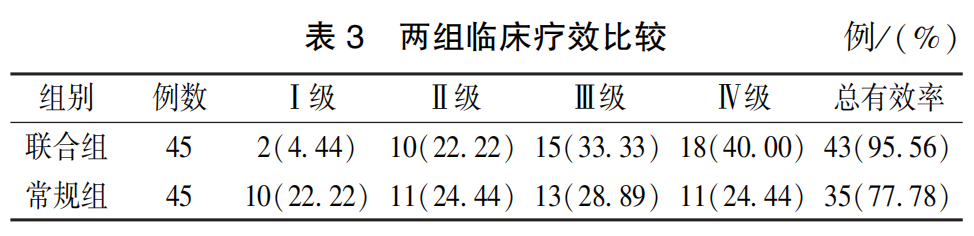
2.1 两组临床疗效比较
联合组疗效为 95. 56%(43 / 45),常规组为 77. 78%(35 / 45),差异有统计学意义( χ2= 6. 154,P = 0. 013),见表 3。
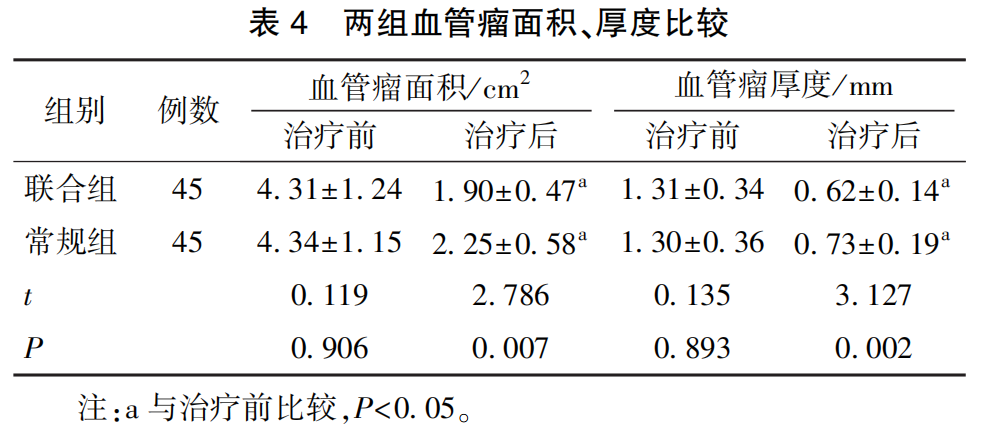
2.2 两组血管瘤面积、厚度比较
治疗前,两组患儿血管瘤状态如血管瘤面积、厚度比较差异无统计学意义(P>0. 05)。 治疗后,两组患儿血管瘤面积、厚度均减小(P<0. 05),且联合组小于常规组(P<0. 05)。 见表 4。
2.3 两组患儿血管生成因子水平比较
治疗前,两组患儿 TGF-β1、bFGF、VEGF 水平比较差异均无统计学意义(P>0. 05)。治疗后,两组患儿 TGF-β1、bFGF、VEGF水平下降( P < 0. 05 ), 联合组 TGF-β1、bFGF、VEGF水平低于常规组(P<0. 05)。 见表5。

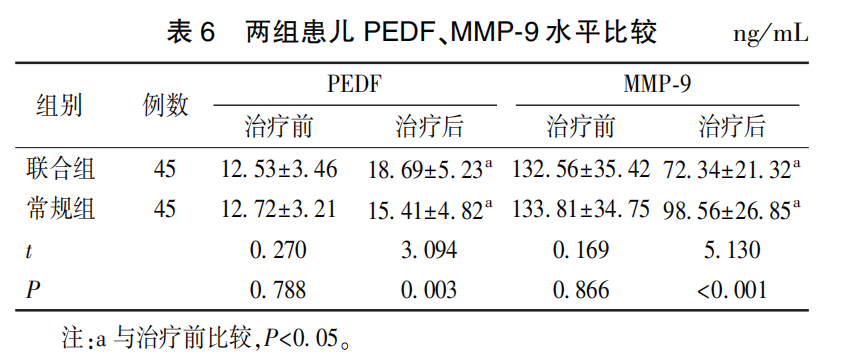
2.4 两组患儿 PEDF、MMP-9 水平比较
治疗前,两组患儿 PEDF、MMP-9 水平比较差异均无统计学意义(P>0. 05)。 治疗后,两组患儿 MMP-9 水平均下降,PEDF 水平升高(P<0. 05);联合组 MMP-9 水平低于常规组,PEDF 水平高于常规组(P<0. 05)。 见表 6。
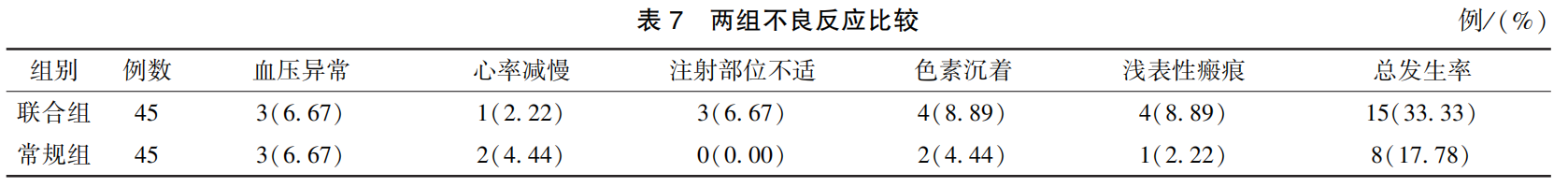
2.5 两组不良反应比较
联合组不良反应发生率为 33. 34% ( 15 / 45),常规组为 17. 78%(8 / 45),差异无统计学意义(χ2= 2. 862,P=0. 091),见表 7。
三、 讨论
IH 治疗方法多样,包括口服糖皮质激素、局部注射平阳霉素或激素、动脉栓塞、冷冻、手术切除等。 常见的激光治疗伴有疼痛,儿童需镇静或麻醉剂配合,且术后存在溃疡、色素沉着、瘢痕等风险[10]。 β 受体阻滞剂可阻断 β 受体,抑制血管内皮细胞增殖及去甲肾上腺素介导的血管扩张,从而抑制瘤体生长[11]。 其中 β1 受体阻滞剂阿替洛尔治疗 IH 的疗效与普萘洛尔相当,且因具亲水性,中枢神经系统不良反应风险较低,故临床应用更广泛[12]。聚桂醇作为硬化剂,注入瘤体后可使血管内皮细胞变性、坏死, 导致血管闭塞, 瘤体纤维化萎缩[13-14]。 有研究[15]显示,聚桂醇联合 β 受体阻滞剂治疗婴幼儿腮腺区血管瘤时,能够抑制环氧合酶-2、结缔组织生长因子及 VEGF 表达,效果良好。 本研究通过对 IH 患儿不同治疗方案进行分析,发现联合疗法治疗后的患儿血管瘤面积和厚度均小于常规治疗患儿。 表明联合治疗能更有效地抑制血管瘤的生长并促使其萎缩。 VEGF是血管生成的关键调节因子,在血管瘤增生期高表达、消退期显著降低,与病情发展密切相关[16-17]。 bFGF 可刺激血管内皮细胞的分裂与增殖活动,促使组织内血管新生增多,或可加重病情[18-19]。 TGF-β1 在血管瘤增殖期可促进血管内皮细胞增殖, 加快细胞外基质合成[20-21]。 本研究联合组患儿治疗后TGF-β1、 bFGF、VEGF 水平下降幅度较常规组更明显。进一步证实联合治疗可通过抑制血管生成相关因子的表达对血管瘤的血管生成发挥强效抑制作用。
多功能蛋白 PEDF 是高效血管形成抑制因子,兼具神经保护、促进肿瘤细胞向神经元分化、促神经干细胞自我更新等功能,在抗肿瘤治疗中发挥着关键作用[22]。PEDF 通过抑制 VEGF 增殖与迁移、诱导细胞凋亡、降低肿瘤细胞的侵袭与转移能力,以及阻断血管新生等多重机制,显著抑制肿瘤的生长,其抗肿瘤作用已在多种癌症治疗中得到验证[23]。 MMP 家族能促进血管内皮生长因子释放,从而刺激新血管形成,还能分解构成血管瘤生长天然屏障的细胞外基质,并参与细胞外基质的重塑过程,上述病理生理变化进一步推动血管生成的进程[24]。 有研究表明,MMP-9 的过表达与 IH 患儿瘤体的增生密切相关,其可能是导致患儿瘤体增生的一个关键风险因素,同时也可作为早期预测和评估患儿瘤体增生风险的重要指标[7]。 治疗后,两组患儿 PEDF 水平升高,MMP-9 水平降低,且联合组在调节上述两个因子方面表现更优。 联合治疗通过调节上述两个关键因子的平衡,更有效地抑制血管瘤的发展。 两组在安全性方面比较差异无统计学意义,联合组不良反应主要表现为血压异常(6. 67%)、心率减慢(2. 22%)、注射部位不适(6. 67%),且伴轻度色素沉着(8. 89%)和浅表性瘢痕(8. 89%),多为轻度且可控,未对治疗进程造成严重影响。 提示 β 受体阻滞剂联合聚桂醇治疗未显著增加系统性风险,虽存在聚桂醇相关的局部反应,但通过超声引导精准注射可有效控制药物分布,总体安全性良好。 本研究主要通过临床影像学与血清学指标评估疗效,而未将病理组织学作为金标准,主要是基于临床实践与伦理考量。 当前国内外诊疗指南均指出,IH 的诊断与随访应优先采用无创、可重复的方法[25]。 血清指标及瘤体形态测量不仅能动态反映病情变化,也具有较好的可操作性及家长接受度,符合真实临床场景下的研究设计需求,因此可作为有效、合理的疗效评价替代指标。 从治疗效果来看,联合组疗效优于常规组。 推测 β 受体阻滞剂可能通过抑制血管内皮细胞增殖控制瘤体进展,联合聚桂醇诱导血管内皮细胞变性坏死、促进瘤体纤维化闭塞的双重机制,可协同加速血管瘤消退,尤其对深部或混合型血管瘤的疗效优势更为显著[26-27]。 进一步证实联合治疗在提高治疗效果、促进血管瘤消退方面的优越性,为临床治疗婴幼儿血管瘤提供了更有效的选择。
综上所述,β 受体阻滞剂联合聚桂醇治疗 IH 的疗效显著,不仅能更有效地减小血管瘤面积和厚度,还能更好地调节血清中与血管生成密切相关因子的水平,安全性良好。 但在实际应用中,仍需密切观察患儿的治疗反应和不良反应,根据个体情况进行合理调整。




